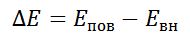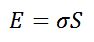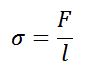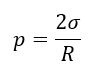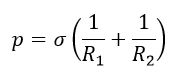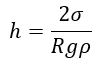Поверхностное натяжение в жидкостях проявляется не только при надувании мыльных пузырей. Эти силы позволяют нам писать чернилами, не промокать под небольшим дождем, а почве сохранять влажность между поливами, растениям поднимать воду к тканям по всей их длине. Мы не могли бы видеть радугу, так как капли, преломляющие свет, не могли бы образоваться.

Поверхностное натяжение– основная термодинамическая характеристика поверхностного слоя жидкости на границе с газовой фазой или другой жидкостью.
Молекулярная картина поверхностного слоя
Молекулы жидкости притягиваются друг к другу силами Ван-дер-Ваальса, но силы их притяжения к молекулам воздуха значительно слабее. Это явление выражается в стремлении жидкости втянуть молекулы поверхностного слоя внутрь и сократить поверхность.
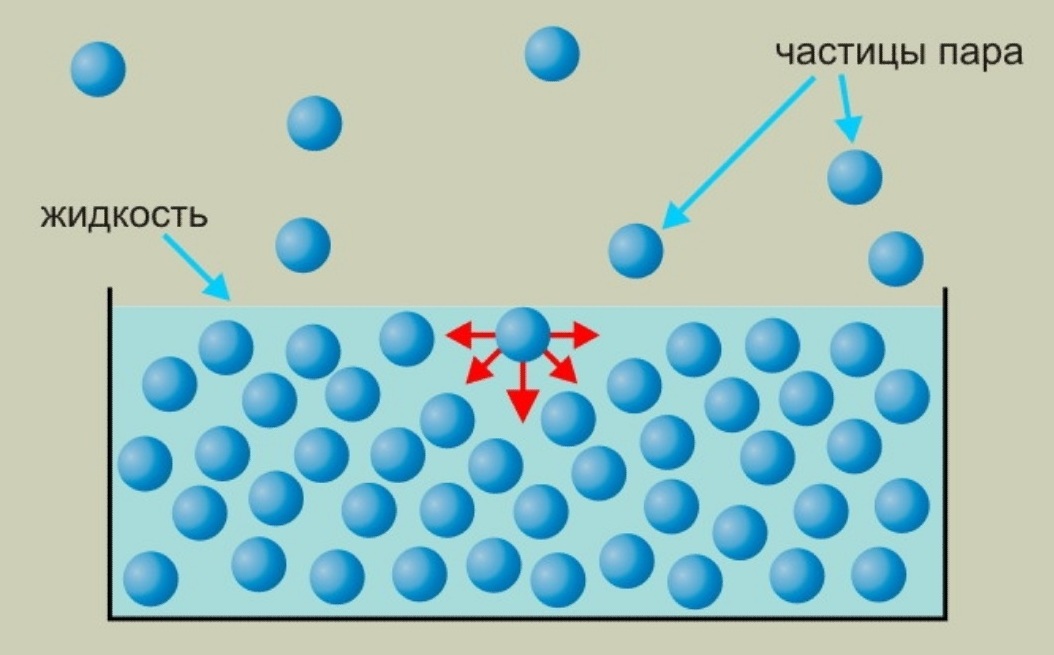
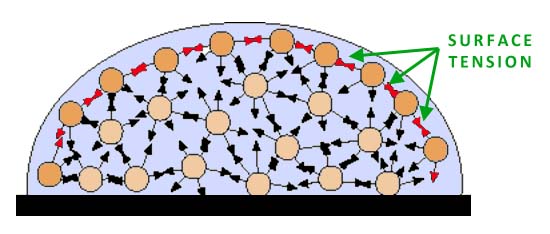
Поверхностная энергия
Свободная поверхностная энергия– это избыток энергии молекул поверхностного слоя по сравнению с молекулами, находящимися внутри
Эта энергия зависит от природы вещества соприкасающихся фаз, от температуры и площади раздела фаз.
Свободная поверхность жидкости – это граница между жидкостью и ее паром. Для того, чтобы перевести молекулу с глубины жидкости не поверхность, нужно совершить работу. Поэтому молекулы на поверхности имеют бОльшую энергию, чем внутри.
Как известно, любая система стремится к минимуму энергии. Чтобы уменьшить свободную поверхностную энергию у системы есть два пути: уменьшить поверхностное натяжение σ или площадь поверхности раздела фаз S.
Уменьшение σ происходит при адсорбции веществ на твердых и жидких поверхностях (это является движущей силой адсорбции), при растекании одной жидкости по другой.
Стремление к уменьшению площади поверхности S приводит к слиянию частиц дисперсной фазы, к их укрупнению.
Стремление жидкости к уменьшению поверхности приводит к тому, что она стремится принять форму шара. Математические расчеты показывают, что наименьшую площадь при постоянном объеме имеет шар, поэтому частицы жидкости принимают шарообразную форму, если только эти капли не расплющиваются под действием силы тяжести. Капли ртути на поверхности приобретают форму шариков. В невесомости все жидкости приобретают форму шара; шарообразную форму планет также приписывают действию поверхностных сил.


Коэффициент поверхностного натяжения σ – это работа, которую надо совершить, чтобы в изотермических условиях увеличить на единицу площадь поверхности раздела фаз при неизменном объеме жидкости(т.е. перенести соответствующее число молекул жидкости из объема в поверхностный слой).
Например, при разбрызгивании жидкости совершается работа, которая переходит в свободную поверхностную энергию (при разбрызгивании поверхность раздела фаз многократно увеличивается).
Так как поверхностное натяжение связано с работой, расходуемой на разрыв межмолекулярных связей при переводе молекул из объема в поверхностный слой, то, очевидно, что поверхностное натяжение является мерилом сил межмолекулярного взаимодействия внутри жидкости.
Сила поверхностного натяжения
Поверхностное натяжение – это сила.
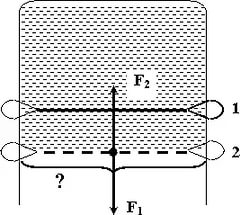 |
Существование этой силы наглядно иллюстрируется опытом Дюпре. На жесткой проволочной рамке закреплена подвижная перемычка. В рамке натянута мыльная пленка (положение 1). Чтобы растянуть эту пленку до положения 2, надо приложить силу F, которой противодействует сила поверхностного натяжения F2. Если отпустить перемычку, то она вернется в прежнее положение 1. Это произойдет под действием силы поверхностного натяжения. Эта сила направлена вдоль поверхности (по касательной), перпендикулярно к контуру, ограничивающему поверхность. Для пленки роль части контура играет подвижная перемычка. |
где F – сила, стягивающая контур поверхности, Н; l – длина контура, м.
Смачивание и несмачивание
При соприкосновении жидкости с твердым телом ее поверхность искривляется по-разному в зависимости от сил взаимодействия между ними.
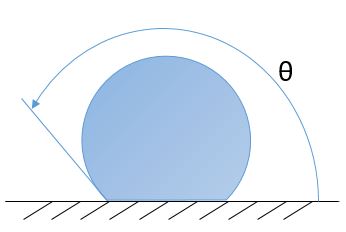
Угол между касательной к поверхности жидкости и твердого тела называется углом смачивания θ. Если θ < π/2, то жидкость смачивающая, а если θ > π/2, то несмачивающая.
| Смачивание – силы притяжения между молекулами жидкости больше, чем между жидкостью и твердым телом | Несмачивание – больше сила притяжения между молекулами жидкости и твердого тела |
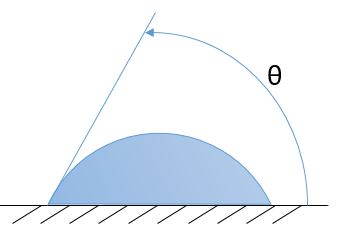 |
 |
Смачивание и несмачивание – понятия относительные. Жидкость может смачивать одну поверхность и не смачивать другую.
Капиллярные явления
Капилляр – это тонкая трубка, в которой жидкость может подниматься или опускаться в зависимости от смачивания или несмачивания.
Капиллярные явления – явления изменения высоты жидкости в тонких трубках по сравнению с широкими сосудами.
В трубках с узким сечением поверхность жидкости имеет вид сферы (мениск). Если жидкость смачивающая поверхность сосуда, то образуется вогнутый мениск, если несмачивающая – выпуклый.
Если поверхность жидкости вогнутая, то давление жидкости под ней меньше, поскольку силы поверхностного натяжения направлены из жидкости по касательной к поверхности.
Лапласово давление (давление под поверхностью жидкости) – дополнительное давление, создаваемое силами поверхностного натяжения.
В общем виде избыточное давление под поверхностью двоякой кривизны определяется:
R1 и R2 – радиусы кривизны двух взаимно перпендикулярных сечений жидкости. Радиус положителен, если центр окружности находится внутри жидкости.
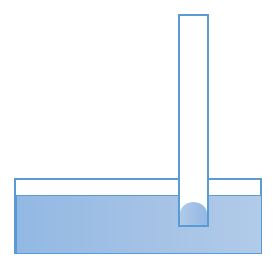
Если узкую трубку с открытым концом поместить в жидкость, то жидкость из-за избыточного давления под поверхностью будет подниматься (если жидкость смачивающая) или опускаться (если жидкость несмачивающая), так как избыточного давления нет.
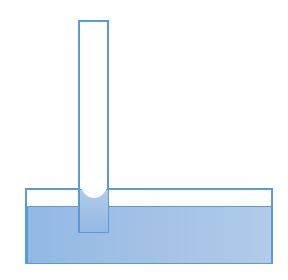
Жидкость поднимается или опускается на такую высоту, на которой выравниваются давления столба жидкости и избыточное давление за счет поверхностного натяжения:
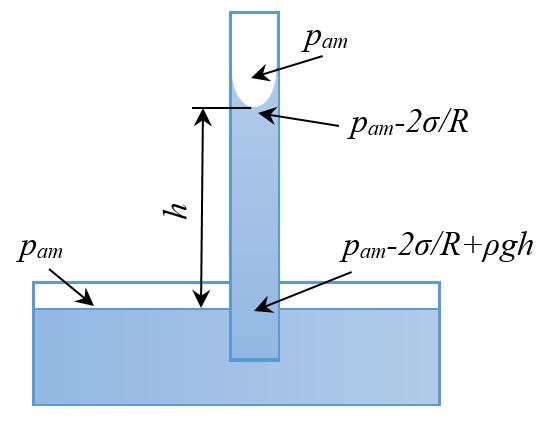
Распределение давлений внутри капилляра