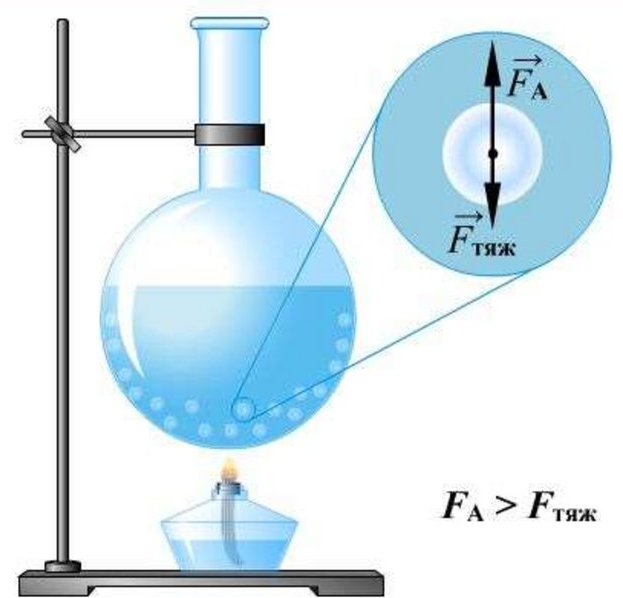
При нагревании воды в сосуде на дне и стенках сосуда образуются пузырьки. Это пузырьки воздуха, который всегда растворён в воде. Кроме воздуха, в пузырьках находится насыщенный пар, который образуется при испарении воды внутрь этих пузырьков.
Так как вода в верхних слоях ещё не прогрелась, пар в пузырьках остывает и конденсируется. В результате они резко сжимаются (схлопываются), и мы слышим, как вода шумит. Когда вода прогревается по всему объёму, поднимающиеся пузырьки уже не уменьшаются в размерах. Достигая поверхности воды, они лопаются, выбрасывая наружу водяной пар. Таким образом происходит кипение.
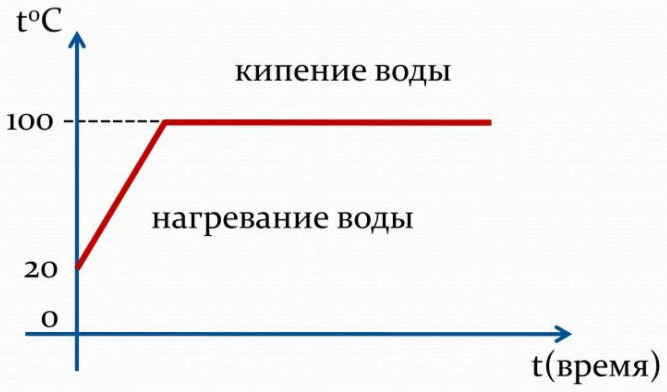
Кипение — это процесс парообразования, происходящий по всему объёму жидкости.
Кипение происходит при такой температуре, при которой давление насыщенного пара равно давлению внутри жидкости. Температура жидкости во время кипения не меняется.
Температуру, при которой жидкость кипит, называют температурой кипения.
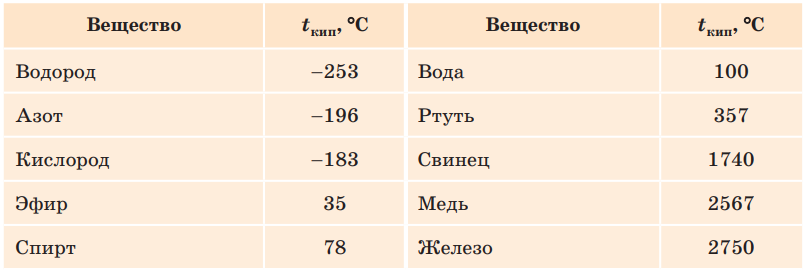
Температура кипения некоторых веществ (при нормальном атмосферном давлении)
Летучие жидкости — эфир, спирт — кипят при сравнительно низких температурах. Это объясняется малыми силами взаимодействия между молекулами. Поэтому нужно лишь небольшое нагревание, чтобы давление паров летучих жидкостей достигло атмосферного. Давление же паров ртути становится равным атмосферному лишь при температуре 357ºС. При комнатной температуре оно мало.
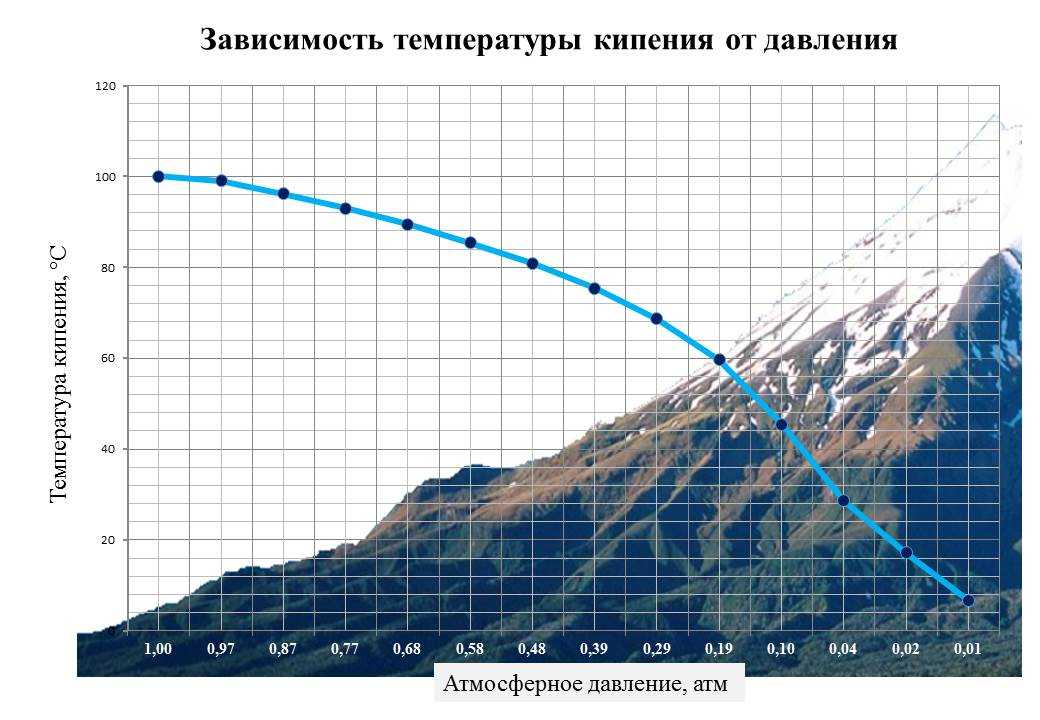
Температура кипения зависит от атмосферного давления. При увеличении атмосферного давления температура кипения повышается, при уменьшении — понижается. Это следует из условия кипения. Чем больше атмосферное давление, тем при более высокой температуре давление внутри пузырьков с ним сравняется.
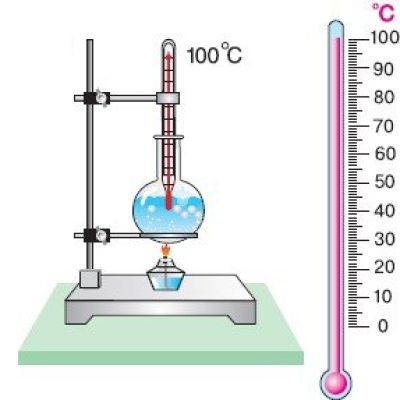
Если термометр во время опыта поместить над поверхностью кипящей воды, то окажется, что температура пара равна также 100ºС. Это означает, что кинетическая энергия молекул при кипении остаётся неизменной. На что же расходуется подводимая к жидкости энергия?
Энергия идёт на увеличение потенциальной энергии молекул. Ведь для того, чтобы превратить жидкость в пар, нужно совершить работу по удалению притягивающихся друг к другу молекул на значительные расстояния.
Таким образом, внутренняя энергия пара больше внутренней энергии воды, из которой он образовался. Этим объясняется тот факт, что ожог паром бывает более тяжёлым, чем кипятком при температуре 100ºС.